2019年国内PD-L1可以报销医保吗?纽约外地工夫11月18日,辉瑞公司宣布,FDA已同意该公司申报的Abrilada 上市。Abrilada是一款Humira的生物相似药,该药物的获批,也使得辉瑞公司拥有的获批生物相似物到达6个,成为拥有最多生物相似药产品组合的公司之一。
在Abrilada 获批之前,FDA药品审评与研讨中心生物制品与生物相似药办公室代理主任Sarah Yim医生地下宣布声明,表示FDA将继续推进生物制品竞争,同时引见了FDA在生物相似药审评方面展开的一系列重要任务。以下为Yim医生的声明全文。
生物相似物:提供更多医治途径,降低医治费用
生物制品在古代医学中发扬着越来越重要的作用,为多种严重疾病提供了无效的医治手腕。这些运用先进技术开发的生物制品,通常来自于自然或无机体,例如植物和植物细胞;有的来源于微生物,例如细菌或酵母。与小分子药品相比,生物制品更为复杂;在医治癌症和本身免疫疾病方面,例如风湿性关节炎、银屑病与炎症性肠炎,尤其显得重要。
历史上,由于没有简化的FDA审评途径将“跟随式”生物制品推向市场,因而,生物制品市场已经缺乏无效竞争。2010年国会受权FDA针对生物相似药与可互换生物产品展开简化审批通道,使缺乏无效竞争的状况发作了变化。生物相似物审批通道,受权FDA对生物相似药产品审评、审批;这些产品,可以为患者提供更多的医治途径,降低医治费用。生物相似药与FDA同意的生物制品高度相似,在临床上不存在明显差异。FDA为平安、无效的生物相似药产品上市提供支持的才能,关于患者和医疗保健零碎至关重要。
数据来源:参考材料[2]
已同意25个生物相似药
FDA同意Humira的生物相似药Abrilada,进一步促进生物制品竞争。这一同意,是2019年FDA决议予以同意的第9个生物相似药,同时使取得FDA同意的生物相似药总数到达25个。我很快乐看到这一停顿,对这些医治药品的市场持续坚持增长充溢决心。迄今为止,FDA的生物相似药开发方案,已注册了针对38种不同参比生物制品的74个方案。对这些拟推出的生物相似药、可互换产品开发的详细讨论,为保证继续的市场竞争奠定了根底。
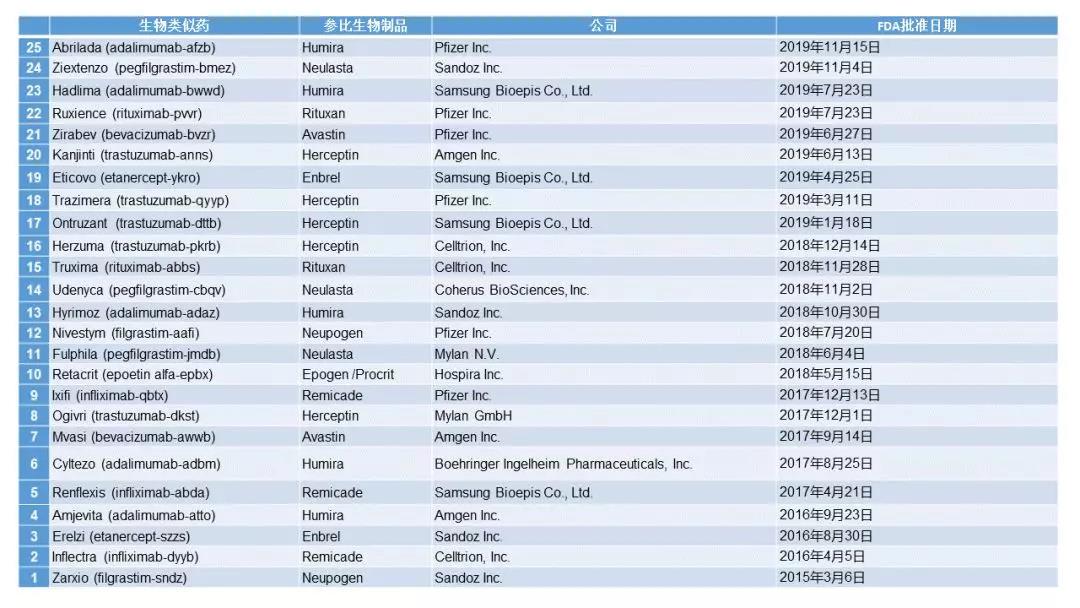
▲迄今为止,FDA同意的25个生物相似药
重要的是,在运用取得FDA同意的生物相似药时,医疗保健专业人士与患者,可以充沛信任这些获批产品。取得FDA同意的生物相似药,都经过严厉审评,以确定这些药品能否契合答应要求,并依照与品牌药相反的质量规范消费。
进一步进步生物相似药开发与审批效率
FDA还根据生物相似药举动方案持续展开任务,进步生物相似药和可互换产品开发与审批流程的效率。这些任务,包括开发与施行新的专门用于生物相似药审评模板的任务;以及针对生物相似药开发量身定制的药效先生物标志物的开发与验证。依照该方案,我们将持续为生物相似药开发者,进一步从迷信与法规的角度予以明白;同时展开沟通和宣贯任务,进步患者对生物相似药的看法,让临床医生和领取方更深化地理解生物相似药的平安性和无效性。
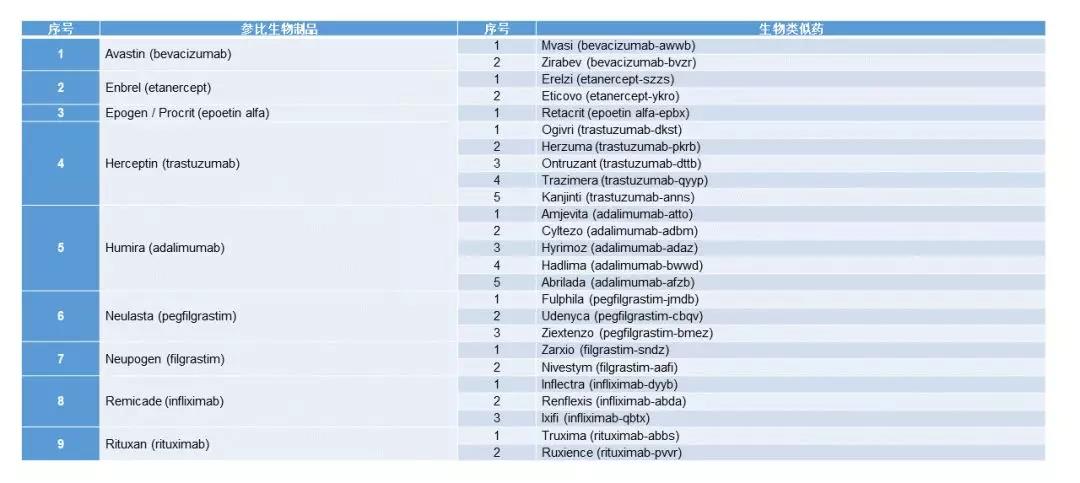
▲FDA同意生物相似药的参比生物制品
NDA转换为BLA
FDA在生物相似物范畴的另一项重要任务,是在美国国会的指点下,将过来根据《联邦食品、药品、化装品法案》上市审批的生物制品,转为根据《公共卫生效劳法案》答应审批的生物制品。这项任务将于2020年3月23日失效,FDA正在努力推进这项任务。这样的转换意味着,这些生物产品,包括胰岛素等需求量大、价钱下跌的产品,将与其它生物制品一样,承受《PHS法案》的监管,并开放给生物相似药竞争。反过去看,这样的转换,能够招致开发更为实惠的生物相似药产品,包括可以与品牌胰岛素互换的产品;这样的产品,不会在平安性和无效性方面有任何妥协。
往年5月份,FDA召开了生物相似药和可互换胰岛素产品开发地下听证会,我们正在剖析从不同的利益攸关方咨询到的建议、意见,包括那些直承受到胰岛素定价影响的人士,以及将受害于生物相似药和可互换产品竞争影响的人士。转换任务在停止中,属于高度优先事项。
在提供添加取得重要疗法的时机方面,生物相似物与可互换生物制品被各界寄予很大希望,FDA将尽其所能,促进这一范畴的竞争。
2019年国内PD-L1可以报销医保吗?
| 上一篇:2019年国内米哚妥林可以报销医保吗? | 下一篇:2019年国内吉妥单抗可以报销医保吗? |




