顶尖学术期刊《自然》昔日上线了来自颜宁教授团队的一篇论文。这项研讨以“放慢评审文章”方式发布,是颜宁团队多年来解构电压门控钙离子通道的又一力作。

Cav介导钙离子进入细胞,参与多种重要的生理进程,包括基因表达、分泌、细胞死亡等。Cav功用异常或紊乱,可招致神经、心血管等多种零碎的疾病。正由于如此,Cav成为了重要的药物研讨靶标。对其构造和功用特征的片面理解,可以为研发人员发现新药提供指点。
多年来,颜宁教授的研讨组在解构Cav通道的征程上屡次获得关键打破。哺乳植物细胞上已鉴定出的Cav有10种亚型,可分为Cav1、Cav2和Cav3三个亚家族。其中对Cav1.1亚基构造的剖析早在数年前接连宣布于《迷信》和《自然》;Cav1.1结合不同拮抗剂和冲动剂的高分辨率构造,则在往年早些时分宣布于《细胞》。这些任务均为了解Cav的机理打下根底。

▲颜宁教授
此次报道的任务中,研讨团队聚焦Cav3.1通道。与高电压激活的Cav1不同,Cav3.1属于低电压激活通道的代表成员,其活化、失活和离子传导特性有其共同的特征。而且,Cav3在序列的分歧性和类似性上与其他两大Cav家族只要20%和45%左右,预示着在蛋白三维构造上也能够有分明差异。
研讨人员应用冷冻电镜技术,测定了重组表达的人类Cav3.1蛋白的构造,分辨率到达3.3埃。这一后果后续可以为疾病相关的Cav3渐变体提供构造反省的框架。
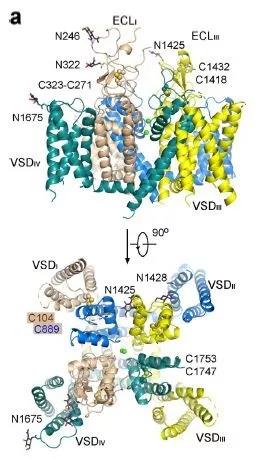
▲人源Cav3.1-Δ8b的构造全貌
此外,研讨团队运用了一种高度选择性的Cav3阻滞剂Z944,捕捉了Cav3.1与Z944相结合时的复合体冷冻电镜构造,分辨率达3.1埃。
Z944是一种已进入2期临床实验的候选药物,用于医治癫痫和神经痛,但是其特异性结合位点和亚型选择性的分子根底过来并不清楚。此次取得的复合物构造显示出,Cav3反复折叠间的膜内启齿是特异性的可成药位点。而结合配体后的构造变化强调,先导化合物与目的蛋白的复合物构造关于药物设计来说至关重要。
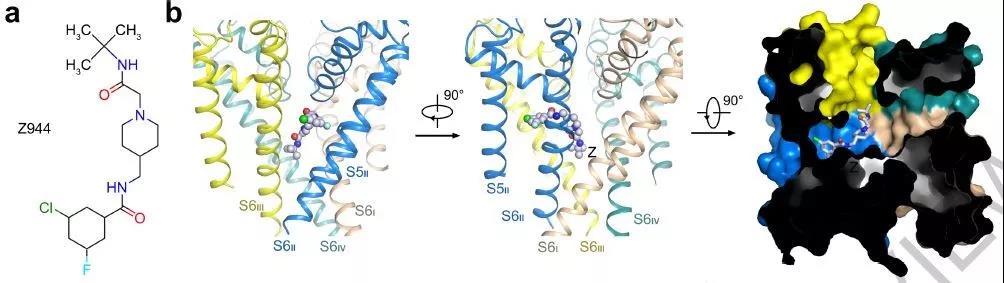
▲特异性阻断剂Z944分子斜插在Cav3通道的空腔中
瞻望将来,正如研讨者在论文最初指出的,解析Cav构造的一系列研讨可以让我们得以比拟不同亚家族之间的特性,“为医治各类Cav通道疾病提供了却构指点药物发现的框架”,有重要指点意义。
| 上一篇:糖尿病一定要趁早治疗! | 下一篇:FDA同意上市世界上首款可减缓儿童远视开展的隐形眼镜 |




