劳拉替尼 “辉瑞一直致力于为ALK阳性非小细胞肺癌患者提供生物标记物驱动药物的先驱,并且在LORVIQUA的批准下,我们将继续推进患者护理,”肿瘤学国际开发市场区域总裁Andreas Penk医师表示。辉瑞 “我们很自豪LORVIQUA是我们在两个月内在欧洲批准的第二种肺癌药物,也是我们第三种由生物标志物驱动的肺癌药物。我们期待将LORVIQUA用于欧洲ALK阳性非小细胞肺癌患者,这些患者已经在使用第二代ALK药物进行了先前的治疗。”
有条件的销售授权基于一项非随机,剂量范围和活动估计,多队列,多中心,1/2期研究B7461001的结果,该评估评估了LORVIQUA用于ALK阳性晚期NSCLC患者的治疗,之前曾接受过一个或多个ALK TKI的患者。在研究的第2阶段部分入组了总共139例接受至少一种第二代ALK TKI(如艾来替尼,布里亚替尼或塞立替尼)治疗的ALK阳性转移性NSCLC的患者。在这些患者中,先前接受过一次ALK TKI治疗的患者的总缓解率(N = 28)为42.9%(95%CI:24.5,62.8)和39.6%(95%CI:30.5,49.4) ),适用于接受过两次或更多次ALK TKI治疗的患者(N = 111)。
“在过去的十年中,我们对ALK阳性非小细胞肺癌的认识得到了极大的发展,从而为患者提供了多种药物。然而,与治疗该疾病相关的常见挑战,包括耐药性和脑转移瘤,迫切需要其他治疗选择,”瓦尔德希伯伦大学瓦尔德希伯伦大学医院Enriqueta Felip博士西班牙肿瘤科。“ LORVIQUA批准标志着肺癌创新的激动人心的时刻,我期待使用这种下一代ALK抑制剂治疗我的患者。”
在B7461001研究中,每天接受一次LORVIQUA 100 mg治疗的295名ALK阳性或ROS1阳性转移性NSCLC患者中,最常见(≥20%)的不良反应是高胆固醇血症(84.4%),高甘油三酸酯血症(67.1%),水肿(54.6%) ),周围神经病变(47.8%),认知影响(28.8%),疲劳(28.1%),体重增加(26.4%),关节痛(24.7%),情绪影响(22.7%)和腹泻(22.7%)。
有条件的批准将授予满足未满足的医疗需求的药品,如果该产品的受益风险风险为正,并且该产品可立即获得的收益超过了缺乏全面数据的风险(通常情况下除外)。1根据有条件批准的规定,辉瑞将提供上市后研究的更多数据,包括正在进行的ALK阳性NSCLC患者一线治疗中LORVIQUA与克唑替尼的3期CROWN研究。
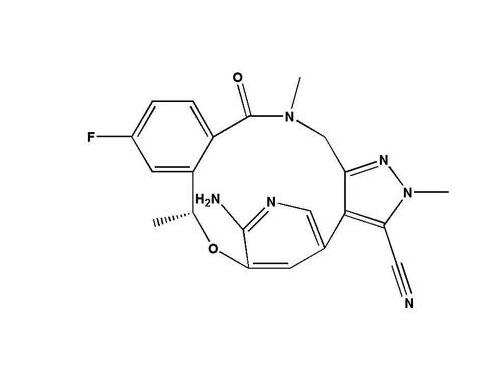
关于LORVIQUA ®(lorlatinib)
LORVIQUA是一种TKI,在具有ALK染色体重排的临床前肺癌模型中已显示出很高的活性。LORVIQUA是专门为抑制导致对其他ALK抑制剂产生抵抗力并穿透血脑屏障的肿瘤突变而开发的。LORVIQUA在欧盟被批准作为单一疗法用于治疗ALK阳性晚期非小细胞肺癌的成年患者,该患者在以下情况下已发展:
alectinib或ceritinib是第一个ALK TKI治疗方法;要么
克唑替尼和至少一种其他ALK TKI。
LORVIQUA也被批准:
以商标名LORBRENA ®在日本用于治疗ALK融合基因阳性不可切除的晚期和/或复发性NSCLC的阻力或不耐受ALK酪氨酸激酶抑制剂。
旗下品牌LORBRENA ®在加拿大,在那里它被有条件地批准作为单药治疗的成年患者ALK阳性转移性NSCLC谁对进展的治疗:克里唑蒂尼和至少一个其他ALK抑制剂,或病人谁对ceritinib或进展艾乐替尼。
旗下品牌LORBRENA ®在美国的患者ALK阳性的转移性NSCLC患者,其疾病进展的治疗:
克唑替尼和至少一种其他ALK抑制剂用于转移性疾病; 要么
艾乐替尼作为首个用于转移性疾病的ALK抑制剂疗法;要么
ceritinib是首个用于转移性疾病的ALK抑制剂疗法。
根据肿瘤反应率和反应持续时间,US适应症获得了加速批准。对于该适应症的持续批准可能取决于验证性试验中对临床益处的验证和描述。
LORBRENA®(lorlatinib)来自美国的重要安全信息处方信息
禁忌症:服用强CYP3A诱导剂的患者禁用LORBRENA,因为它具有严重的肝毒性的潜力。
并用强效CYP3A诱导剂引起严重肝毒性的风险: 接受单剂LORBRENA和每日多次利福平(一种强CYP3A诱导剂)的12位健康受试者中有10位发生严重肝毒性。50%的受试者发生4级ALT或AST升高,33%的受试者发生3级,8%的受试者发生2级。在开始LORBRENA之前,中断强效CYP3A诱导剂的3次血浆半衰期,直到强效CYP3A诱导剂。避免将LORBRENA与中度CYP3A诱导剂同时使用。如果不能避免同时使用中度CYP3A诱导剂,则在开始LORBRENA的48小时后和开始LORBRENA的第一周内至少监测3次AST,ALT和胆红素。根据每种药物的相对重要性,
中枢神经系统(CNS)的影响:可能发生多种中枢神经系统的影响。这些包括癫痫发作,幻觉以及认知功能,情绪(包括自杀观念),言语,精神状态和睡眠的变化。停药并以相同或减少的剂量继续服用,或根据严重程度永久停药。
高脂血症:血清胆固醇和甘油三酸酯可能增加。在接受LORBRENA的332例患者中,总胆固醇的3或4级升高发生,甘油三酸酯的3或4级升高发生在17%。80%的患者需要开始降脂药物治疗,开始这种药物治疗的中位时间为21天。在高脂血症患者中开始或增加降脂药的剂量。在开始LORBRENA之前,开始LORBRENA后1个月和2个月以及此后定期监测血清胆固醇和甘油三酸酯。首次出现时以相同剂量戒断并恢复;以相同或减少剂量的LORBRENA恢复,以根据严重程度复发。
房室传导阻滞: PR间隔延长和AV传导阻滞可能发生。每天接受一次口服100 mg剂量的LORBRENA并进行了基线心电图检查(ECG)的295例患者中,有1%经历了房室传导阻滞,有0.3%经历了3级房室传导阻滞,并接受了起搏器放置。在启动LORBRENA之前和之后定期监测ECG。对于接受起搏器放置的患者,应减少剂量或以相同剂量戒断并恢复。没有起搏器的患者将永久停止复发。
间质性肺疾病(ILD)/肺炎:可能发生与ILD /肺炎一致的严重或危及生命的肺部不良反应。1.5%的患者发生ILD /肺炎,其中1.2%的患者患有3级或4级ILD /肺炎。对于任何表现出指示ILD /肺炎的呼吸道症状加重的患者,应及时调查ILD /肺炎。如果怀疑患有ILD /肺炎,应立即停用LORBRENA。永久中断LORBRENA治疗任何严重程度的与治疗相关的ILD /肺炎。
胚胎胎儿毒性: LORBRENA可引起胎儿伤害。 建议孕妇注意胎儿的潜在危险。建议具有生殖潜力的女性使用有效的非激素避孕方法,因为在用LORBRENA治疗期间以及最终剂量后至少6个月内,LORBRENA可使激素避孕药无效。建议具有生殖潜能的女性伴侣的男性在接受LORBRENA治疗期间以及最终剂量后的3个月内使用有效的避孕方法。
不良反应: 295例患者中有32%发生严重不良反应。最常见的严重不良反应是肺炎(3.4%),呼吸困难(2.7%),发热(2%),精神状态改变(1.4%)和呼吸衰竭(1.4%)。致命不良反应发生在2.7%的患者中,包括肺炎(0.7%),心肌梗塞(0.7%),急性肺水肿(0.3%),栓塞(0.3%),周围动脉闭塞(0.3%)和呼吸窘迫( 0.3%)。最常见的不良反应(≥20%)为水肿,周围神经病变,认知障碍,呼吸困难,疲劳,体重增加,关节痛,情绪障碍和腹泻。最常见的实验室异常(≥20%)是高胆固醇血症,高甘油三酯血症,贫血,高血糖症,AST升高,白蛋白血症,
药物相互作用:服用强效CYP3A诱导剂的患者禁用LORBRENA。避免与中度CYP3A诱导剂和强效CYP3A抑制剂同时使用。如果不能避免同时使用中度CYP3A诱导剂,则按建议监测ALT,AST和胆红素。如果不能避免与强效CYP3A抑制剂同时使用,则按建议减少LORBRENA剂量。并用LORBRENA会降低CYP3A底物的浓度。
哺乳期:由于母乳喂养的婴儿可能会出现严重的不良反应,请指示妇女在用LORBRENA治疗期间和最终剂量后7天不要母乳喂养。
肝功能不全:轻度肝功能不全的患者不建议调整剂量。对于中度或重度肝功能不全的患者,尚未确定推荐的LORBRENA剂量。
肾功能不全:轻度或中度肾功能不全的患者不建议调整剂量。尚未确定严重肾功能不全患者的推荐剂量LORBRENA。
请在此处查看LORBRENA在美国的完整处方信息。
关于非小细胞肺癌
肺癌是全球最常见的癌症,2018年全球诊断出超过200万新病例。2在所有肺癌中,约有85%被鉴定为非小细胞肺癌,其中约75%为转移或晚期肺癌。诊断。3
ALK基因重排是一种遗传变异,可驱动某些患者患上肺癌。4,5流行病学研究表明,约有3-5%的NSCLC肿瘤为ALK阳性。6
关于辉瑞在肺癌中的应用
辉瑞肿瘤学致力于解决肺癌患者的未满足需求,而肺癌是全球癌症相关死亡以及特别难以治疗的疾病的主要原因。辉瑞致力于通过开发有效且可耐受的疗法(包括生物标志物驱动疗法和免疫肿瘤(IO)药剂及其组合)来满足非小细胞肺癌(NSCLC)患者不断变化的需求。通过将领先的科学见解与以患者为中心的方法相结合,辉瑞不断推进其工作,以在合适的时间为合适的患者提供合适的药物。通过不断发展的研究渠道和协作努力,我们致力于为NSCLC病人带来新的希望。
关于辉瑞肿瘤学
在辉瑞肿瘤学,我们致力于在我们认为可以对患者的生活产生有意义的变化的任何地方推进药物开发。如今,辉瑞肿瘤学拥有业界领先的产品组合,包括18种已获批准的创新抗癌药物和生物仿制药,涉及20多种适应症,包括乳腺癌,前列腺癌,肾脏病,肺病和血液病。辉瑞肿瘤学正在努力改变癌症的发展轨迹。
辉瑞公司:携手共创更健康的世界®
在辉瑞公司,我们运用科学和全球资源为人们提供疗法,以延长并显着改善他们的生活。我们努力为保健产品的发现,开发和制造树立质量,安全和价值的标准。我们的全球产品组合包括药品和疫苗以及许多世界上最著名的消费者保健产品。辉瑞公司的同事每天都在发达市场和新兴市场中开展工作,以改善挑战当今时代最令人恐惧的疾病的保健,预防,治疗和治愈方法。根据我们作为全球领先的创新生物制药公司之一的职责,我们与医疗保健提供商合作,政府和当地社区在世界范围内支持和扩大获得可靠,负担得起的医疗保健的机会。150多年来,我们一直致力于为所有依赖我们的人们带来改变。我们会定期在网站上发布对投资者可能重要的信息www.pfizer.com。此外,要了解更多信息,请访问我们的www.pfizer.com ,并按照我们在Twitter上@Pfizer 和 @Pfizer_News, LinkedIn, YouTube的,像我们在Facebook在Facebook.com/Pfizer。
| 上一篇:玻玛西林,FDA批准Opdivo最新使用方法和最全适应症! | 下一篇:劳拉替尼(Lorlatinib)是怎么发挥功效的? |




